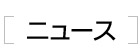スキャンポファーマシューティカルズ社(アメリカ・メリーランド州ベセスダ/ 以下スキャンポ社)、及びアボット社(アメリカ・イリノイ州シカゴ )は、日本人慢性特発性便秘症(Chronic Idiopathic Constipation: CIC)患者を対象とした48週間の第Ⅲ相長期投与安全性・有効性試験において、ルビプロストンの安全性と忍容性を示す良好な成績が得られたことを、2010年11月30日、発表しました。
この第Ⅲ相長期投与試験は、多施設非盲検試験であり、日本人のCIC患者に24μgカプセルを1日2回48週間投与しました。209例が組み入れられ、173例が24週間投与を完了し、163例が48週間投与を完了しました。48週間の投与を完了した患者数は、当初予定していた35例を大きく上回っています。組み入れられた患者は、少なくとも過去6か月の間、1週間当たりの自発排便回数が3回未満であった患者であり、この病歴は14日間のスクリーニング期間中に確認されています。
本試験において、多く見られた副作用は、下痢(37.3%)、悪心(27.3%)、胸部不快感(7.2%)、腹痛(5.3%)であり、いずれも一過性のものでした。副作用の初回発現の多くは、投与開始2週間以内に認められました。多く見られた軽度の副作用は、下痢、悪心、胸部不快感、嘔吐、腹痛、腹部不快感、腹部膨満感であり、また多く見られた中等度副作用は、下痢、悪心、嘔吐、めまいでした。重篤な副作用は認められませんでした。
2009年2月、スキャンポ社はアボット社とルビプロストンの商業化・供給に関するライセンス契約を締結し、これによりアボット社は日本国内においてルビプロストンを慢性特発性便秘症治療薬として独占的に商業化する権利、ならびに日本国内におけるルビプロストンの開発される追加効能に対する優先交渉権を獲得しました。スキャンポ社は引き続き日本でルビプロストンの開発、および規制当局対応を進めてまいります。
「今回得られたデータは過去米国、及び日本で実施された第Ⅲ相試験において得られた安全性、及び有効性のデータと完全に一致しており、非常に喜ばしく思っています。最近実施しました製造販売承認申請の追加データとして、2011年初頭に今回のデータの解析結果を独立行政法人医薬品医療機器総合機構に提出するのを楽しみにしております」とスキャンポ社最高経営責任者兼会長の上野隆司(M.D., Ph. D., Ph.D.)は述べています。
「ルビプロストンの長期安全性データは有望なものであり、日本のCIC患者が近い将来、その困難な状況から解放されるという期待を持てるようになると、我々にも期待させるものです」とアボット ジャパン株式会社代表取締役社長のゲリ-・ワイナ-は述べています。
また東北大学大学院医学系研究科の福土審教授(M.D., Ph.D.)は、「今回の結果は、ルビプロストンが慢性便秘により日常生活の変化を余儀なくされている日本人患者に対し有用な薬剤となりうることを示したものである」と述べています。
さらにミシガン大学内科のWilliam D. Chey教授は、「今回得られたデータは、ルビプロストンが便秘型過敏性腸症候群に罹患している、していないに関わらず、日本人CIC患者にとって安全で有用な治療選択肢であることを示しており、過去に報告されている第Ⅲ相有効性試験の結果とも一致している」と述べています。
今回の長期投与安全性試験で得られた、主要な有効性成績は以下の通りです。
1. 自発排便 (SBM)の回数は、投与前に比べ、投与1週目より統計学的に有意に増加し、
この効果は試験期間中維持された(p<0.001)。
2. リズミックSBMの回数は、投与前に比べ、投与1週目より統計学的に有意に増加し、
この効果は試験期間中維持された(p<0.001)。
3. 65.4%の患者で、初回投与後24時間以内にSBMを認めた。
4. 81.3%の患者で、初回投与後48時間以内にSBMを認めた。
5. 自発排便後の残便感は、投与前に比べ、投与1週目より統計学的に有意に低下し、
この効果は投与期間中維持された(p<0.001)。
6. 便の硬さは、投与前に比べ、投与1週目より統計学的に有意に改善し、
この効果は投与期間中維持された(p<0.001)。
7. 自発排便時のいきみは、投与前に比べ、投与1週目より統計学的に有意に低下し、
この効果は投与期間中維持された(p<0.001)。
8. 腹部膨満感は、投与前に比べ、投与1週目より統計学的に有意に低下し、この効果は
投与3週目にはより高くなり、その後投与期間中維持された(p<0.01およびp<0.001)。
9. 腹部不快感は、投与前に比べ、投与2週目より統計学的に有意に低下し、この効果は
投与3週目にはより高くなり、その後投与期間中維持された(p<0.01およびp<0.001)。
10. 救済薬の使用頻度は、投与前に比べ、投与1週目より低下し、投与2週目には統計学的に
有意な低下が見られた。この効果は投与3週目にはより高くなり、
その後投与期間中維持された(p<0.01およびp<0.001)。
11. QOL評価であるSF-36の4つの下位尺度において、投与前に比べ、統計学的に有意な改善が
見られた(p<0.01)。この4つの下位尺度は、身体機能、体の痛み、全体的健康感、
日常役割機能(精神)で、投与前、投与24週目、及び48週目に患者の自記回答で実施した。
12. QOL評価であるIBS-QOL-Jの9つの下位尺度において、投与前に比べ、統計学的に有意な
改善が見られた(p<0.001)。この9つサブスケールは憂うつ、活動制限、ボディーイメージ、
健康に対する心配、食事回避、社会生活、性的問題、人間関係、身体機能で、投与前、
投与24週目、及び48週目に患者の自記回答で実施した。
今回の試験で得られたデータは更なる解析を現在実施中で、今後、適切な学会にて発表予定です。
スキャンポ社は、ClC患者の治療薬として日本においてルビプロストンを開発しています。
2010年9月、スキャンポ社はCICを適応症としてルビプロストン24 μgカプセルの
製造販売承認申請を独立行政法人医薬品医療機器総合機構に提出しました。今回発表したデータの
全解析結果は、この申請の追加データとして、2011年初頭に提出する予定です。
第Ⅲ相有効性試験について
日本人CIC患者を対象とした第Ⅲ相有効性検証試験において、主要評価項目でルビプロストンが統計学的に有意な改善(p<0.001)を示したこと、またその安全性プロファイルがこれまでに得られている臨床試験成績と一致したものであったことは以前に発表した通りです。この試験における主要評価項目は、投与開始後1週間における自発排便回数の変化でした。このプラセボ対照の二重盲検試験では、ルビプロストン24 μgまたはプラセボカプセルを1日2回、28日間投与した124名の日本人CIC患者で評価を実施しました。
慢性特発性便秘症について
便秘症は低頻回、かつ困難を伴う排便状況と規定され、12ヶ月間に12週間以上の便秘症状が
継続した場合に慢性化したと考えられます。慢性便秘において、その原因が他の疾患によらない、
または薬剤によらない場合を特発性となります。慢性特発性便秘症の症状には、いきみ、硬便、膨満感、腹部痛・腹部不快感も含まれます。慢性特発性便秘症の誘因には、水溶性・非水溶性の食物繊維の摂取不足、運動不足、腸障害、腹圧低下や筋力低下などがあります。
スキャンポ社について
Sucampo Pharmaceuticals, Inc.は米国メリーランド州ベセスダ市を拠点とするバイオファーマシューティカルであり、プロストン技術を基盤とした医薬品の開発・商業化を目指しています。プロストンは体内で脂肪酸から酵素15-PGDHにより産生される物質であり、その疾患治療への応用可能性は最高経営責任者兼会長である上野隆司博士により、最初に発見されました。上野博士は1996年に久能祐子博士(現取締役、Advisor, International Business Development)とともに、スキャンポ社を設立いたしました。
詳細については www.sucampo.comをご覧ください。
アボット社について
米国イリノイ州シカゴに本拠を置くアボットは、広範囲のヘルスケアに基盤を置く世界的規模の会社であり、事業内容は新薬の研究・開発に加え、医療用医薬品、栄養剤、医療用機械器具、医療用計測器、診断薬の分野における研究、開発、製造、マーケティングそして販売と多岐にわたっています。グループ総従業員数約9万人を擁し、世界130カ国で営業活動を行っています。
アボット社のニュースリリース、その他情報については、www.abbott.comをご覧ください。
Amitiza(ルビプロストン)の慢性特発性便秘症及び
便秘型過敏性腸症候群への使用について*
*米国のみ該当
Amitiza(ルビプロストン)は、成人の慢性特発性便秘症(24 μg、1日2回)、及び18歳以上の女性の便秘型過敏性腸症候群(8μg、1日2回)の治療薬として処方されています。
Amitizaは器質性の消化管閉塞に対しては禁忌です。器質性消化管閉塞が疑われる患者はAmitizaの服用開始前に、必ず医療提供者による検査を受け、このような障害が無いことを確認してください。
ヒトでの妊婦に対する安全性は確立していません。治療の利益が、胎児への潜在的リスクを上回る時のみ、妊娠期間中に使用してください。妊娠可能な女性の場合、Amitiza処方開始前に、妊娠検査を実施し、有効な避妊を行ってください。
Amitizaの服用により悪心が起こるかもしれません。もし起こった場合には、Amitizaを食事と
一緒に服用することで、この悪心症状が抑えられる可能性があります。重篤な悪心が起こった場合には、医療提供者にお知らせください。
Amitizaは重篤な下痢が認められる患者には処方できません。治療中に下痢が発生する可能性が
あることを理解頂き、下痢が重症化した場合には、医療提供者にお知らせください。
Amitizaの服用により最初の服用から1時間以内に呼吸困難が起こる可能性があります。この症状は一般には3時間以内に収まりますが、再度服用した際に発生する可能性もあります。呼吸困難が起こった場合には、医療提供者にお知らせください。これまでに、呼吸困難により、投与を中止した患者もいます。
慢性特発性便秘症の患者を対象としたAmitizaの臨床試験(24μg、1日2回投与 vs.
プラセボ:N=1113 vs. N=316)において、高頻度(発生率>4%)にみられた副作用は、悪心(29% vs. 3%)、下痢(12% vs. 1%)、頭痛(11% vs. 5%)、腹部痛(8% vs. 3%)、腹部膨満感(6% vs. 2%)、鼓腸(6% vs. 2%)でした。
便秘型過敏性腸症候群の患者を対象としたAmitizaの臨床試験(8μg、1日2回投与vs. プラセボ:N=1011 vs. N=435)において、高頻度(発生率>4%)にみられた副作用は、悪心(8% vs. 4%)、下痢(7% vs. 4%)および腹部痛(5% vs. 5%)でした。
Amitizaの処方に関する詳細については www.amitiza.comをご覧ください。
Amitiza®はスキャンポファーマシューティカルズ社の登録商標です。
将来の見通しに関する記述
Sucampo Pharmaceuticalsの将来的な期待、計画、および見通しに関する本プレスリリース中の記述は、いずれもThe Private Securities Litigation Reform Act of 1995の条項に基づく将来の見通しに関する記述です。将来の見通しに関する記述は「プロジェクト」、「考え」、「予想」、「計画」、「期待」、「推定」、「意図」、「~のはずである」、「~であろう」、「~し得る」、「~するつもりである」、「~するかもしれない」、およびその他同様な表現により明示されている場合があります。将来の見通しに関する記述には、特定の適応を治療する場合のAmitizaの潜在的な有用性が含まれます。実際の結果は、2009年12月31日を末日とする年度のフォーム10-Kを含む年次報告書、およびその他米国証券取引委員会(SEC)に提出した書類をはじめとする、Sucampo PharmaceuticalsによるSECへの報告書に記載された項目を含めたさまざまな重要な要因により、本プレスリリース中の将来の見通しに関する記述によって示された結果からは大きく異なる場合があります。本プレスリリース中の将来の見通しに関する記述はいずれも本プレスリリースの日付現在のSucampo Pharmaceuticalsの観点を示したものであり、それ以降の日付時点における観点を示すものとして依存すべきではありません。Sucampoは新たな情報、将来のできごと、あるいはその他のいかなる理由によっても、ただし法によって求められるものを除き、いずれの将来の見通しに関する記述についても更新する義務を負いません。
#この件に関する問い合わせ先
Kate de Santis Alysa Hackett
Sucampo Pharmaceuticals, Inc. Abbott
+1-240-223-3834(米国) +1-847-938-8446(米国)
John Woolford アボット ジャパン株式会社
Westwicke Partners 広報部
+1-410-213-0506(米国) (03)4588-6402