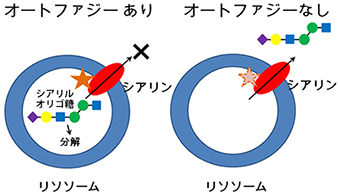
私たちの細胞の中や細胞と細胞の間は、タンパク質、脂質、糖質、核酸などの生体分子で構成されています。これらの分子はずっと新鮮なわけではなく、そのほとんどは約2カ月間で新しいものと入れ替わっているそうです。このため、生体内には不要になったタンパク質や脂質、損傷を受けた細胞小器官などを分解する仕組みがあり、これをオートファジー(自食作用)と呼んでいます。オートファジーの役割には二通りあります。細胞が栄養不足になったときに急激に起きるオートファジーがよく知られていますが、日常的に静かに一定のペースで働いている「基底オートファジー」もあり、細胞内のタンパク質をいつも新鮮に保つ役割をはたしています。これがうまく働かないと細胞内に“ゴミ“が溜まることになり、疾病を引き起こす原因になるとされています。
生物の細胞質には、タンパク質や脂質などと結合しない“遊離”状態の糖鎖(遊離糖鎖)が存在することが古くから知られています。糖鎖はタンパク質をはじめとする生体分子に結合することで特定の機能を与えて、生体内の重要な生理機能を維持しています。しかし、遊離糖鎖が生成、分解される分子メカニズムについて未だ不明でした。そこで、共同研究グループは、糖鎖分解・代謝のメカニズムを突き止めるためにオートファジーに着目しました。
研究グループは、オートファジー経路に必須の遺伝子を欠損させた細胞を用いて、細胞質にどのような糖鎖が蓄積しているかを調べました。その結果、シアル酸という糖をもつ遊離糖鎖「シアリルオリゴ糖」が蓄積していることを発見しました。通常、シアリルオリゴ糖はリソソームで分解され、単糖になったシアル酸が細胞質へ放出されるので、シアリルオリゴ糖そのものは細胞質に蓄積されません。即ち、シアリルオリゴ糖の蓄積に基底オートファジーが重要な関わりをもっていることが示されました。さらに解析を進めたところ、基底オートファジー機能が欠損すると、リソソーム膜上にあるシアル酸を細胞質へ輸送する膜タンパク質「シリアン」が機能変化し、シアル酸ではなくシアリルオリゴ糖を細胞質に放出して蓄積させる可能性が示されました。これにより、基底オートファジー機能が特定の糖鎖の代謝に関わり、リソソームが正常に働くために重要な役割をもつことが明らかになりました。
理研の研究チームは、以前から糖鎖の代謝経路についてリソソーム以外で起きることを提唱していました。今回の研究は、その仮説に基づいて細胞質内の糖鎖の代謝の仕組みを調べていたところ、結局リソソームでの正常な糖鎖代謝の重要性を見つけることになりました。想像した通りにいかないのが研究の醍醐味です。
最近、がん組織にシリアルオリゴ糖が蓄積していることが複数報告されています。これは、シアリルオリゴ糖がさまざまながん種に対するマーカーとして利用できる可能性を示しています。また、基底オートファジーの機能不全が、ある種の細胞のがん化のメカニズムと密接に関わっていることを示唆しています。今後、基底オートファジー欠損下で起こるシアリルオリゴ糖の詳細な分子メカニズムの解明を目指します。
※詳細は下記URLをご参照ください
◎独立行政法人理化学研究所 2013年7月24日発表
http://www.riken.go.jp/pr/press/2013/20130724_1/digest/