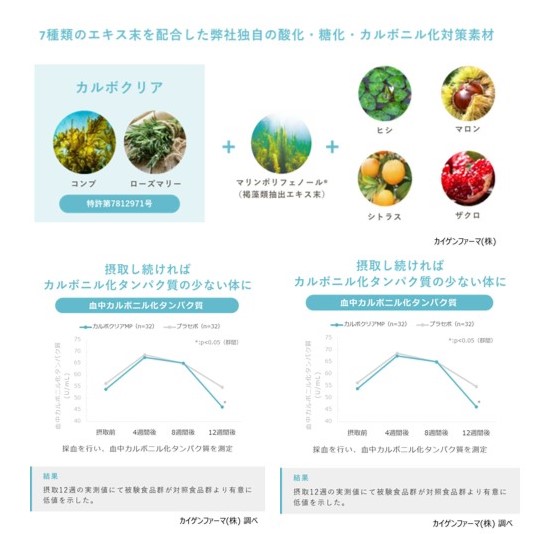
森永乳業は、このたび米国において、ビフィズス菌M-16V(ビフィドバクテリウム・ブレーベ M-16V)が、食品の安全性に関する審査制度であるGRASを取得したことをお知らせいたします。
健康な赤ちゃんのおなかの中はほとんどがビフィズス菌で占められており、特にビフィドバクテリウム・ブレーベ(Bifidobacterium breve)が多くすんでいることが知られています。ビフィズス菌 M-16Vは健康な乳児から分離したビフィドバクテリウム・ブレーベの一種で、同社においてプロバイオティクスとして開発されています。今回、ビフィズス菌M-16Vは、一般食品と育児粉乳の2つの用途で個別に認証を取得し(GRAS Notice No. GRN453, GRN454)、非常に安全な菌であることが証明されました。
ビフィズス菌 M-16Vについては、これまでに低出生体重児において、腸内細菌叢の形成促進、感染症発症の抑制、経腸栄養の早期確立、入院期間の短縮などの作用が示されております。また、アトピー性皮膚炎患児において腸内細菌叢が正常化し、アトピー性皮膚炎症状が改善されるなど抗アレルギー作用も示唆されています。これらの研究成果は、低体重出生児等の臨床試験を含めて合計約30報以上の科学論文において発表されています。
なお、森永乳業はこのビフィズス菌M-16Vを独自技術により高菌数で保存生残性の優れた菌末製品とすることに成功し、乳児用食品に使用しているだけでなく、育児粉乳、健康食品およびサプリメント用の機能性素材として、国内外に販売しています。
米国において、プロバイオティクス市場が成長しているなかで、ビフィズス 菌M-16Vはこれまでも食品やサプリメントの機能性素材として採用されております。今回の承認によって、初めて育児粉乳への利用が可能になりましたので、それら分野を含め広範な一般食品分野への採用が期待されます。また、今後米国を始めその他の多くの地域で広く利用されるよう努めてまいります。
※詳細は下記URLをご参照ください
◎森永乳業 2013年12月5日発表
http://www.morinagamilk.co.jp/download/index/10576/1312052.pdf